Artigos
Pfizer formaliza pedido na Anvisa para uso da vacina da Covid em crianças entre 5 e 11 anos
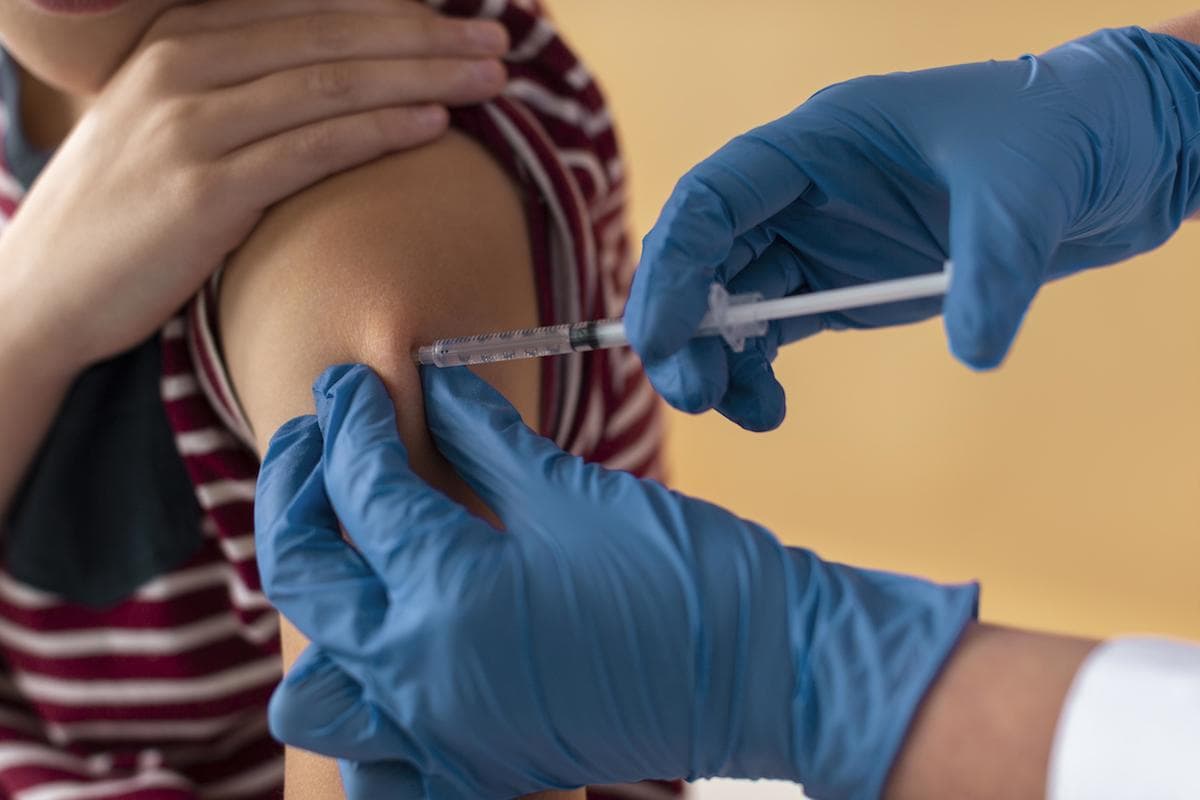
A Agência Nacional de Vigilância Sanitária (Anvisa) informou que recebeu nesta sexta-feira (12) solicitação da Pfizer para incluir a faixa etária de 5 a 11 anos na indicação da sua vacina Comirnaty contra a Covid-19. De acordo com a Anvisa, o pedido da Pfizer prevê que a dosagem da vacina para a faixa etária será ajustada e menor que aquela utilizada por maiores de 12 anos. Dessa forma, a proposta é ter frascos diferentes, com dosagem específica para cada grupo – maiores ou menores de 12 anos. Segundo o laboratório, os frascos serão diferenciados pela cor.
A agência afirmou em nota que “a análise técnica será feita de forma rigorosa e com toda a cautela necessária para a inclusão das crianças menores entre os vacinados”. O prazo de avaliação da solicitação pela Agência é de até 30 dias.
Na terça-feira (10), a Pfizer se reuniu com a Anvisa em uma reunião de pré-submissão dos dados, que antecede o pedido formal, para apresentação geral dos principais dados sobre o imunizante. Segundo a Anvisa, o objetivo dessa reunião é antecipar questões e dar mais agilidade à análise do processo.
A vacina da Pfizer está registrada no Brasil desde 23 de fevereiro deste ano. O registro inicial contemplou pessoas com mais de 16 anos. No dia 11 de junho, a Anvisa autorizou a inclusão da faixa etária de 12 a 15 anos. O imunizante foi considerado 90,7% eficaz na prevenção da Covid-19 na faixa etária infantil. Sobre segurança, um estudo em andamento constatou que não houve nenhum efeito colateral sério em cerca de 3,1 mil crianças de 5 a 12 anos de idade que receberam a vacina da Pfizer.
Nos Estados Unidos, o uso da vacina em crianças entre 5 e 11 anos foi autorizado no último dia 2 e cerca de 400 mil crianças já receberam o imunizante.
Como é feita a análise
A solicitação de inclusão de uma nova faixa etária, ou seja, uma nova indicação na bula, deve ser feita pelo laboratório desenvolvedor da vacina. Para incluir novos públicos na indicação de uma bula, o laboratório precisa conduzir e apresentar estudos que demonstrem a relação de segurança e eficácia da vacina para a nova faixa etária.
No caso de vacinas para o público infantil, alguns dos principais pontos de atenção da Anvisa se referem aos dados de segurança e eventos adversos identificados, ajuste de dosagem da vacina, fatores específicos dos organismos das crianças em fase de desenvolvimento, entre outros.
Resposta mais vigorosa nas crianças
Em coletiva de imprensa online promovida pela Pfizer nesta quarta-feira (11), para divulgação de estudo sobre percepção da população com o avanço da vacinação, o pediatra e infectologista Renato Kfouri, diretor da Sociedade Brasileira de Imunizações (SBim) disse que a expectativa de proteção das crianças menores com a vacinação é grande maior ainda do que em adultos. “Quando a gente vacina crianças menores, a resposta é mais vigorosa no sistema imune, então a gente pode usar uma concentração menor do imunizante e um número menor de doses”, ressaltou Kfouri. Ele disse ainda que por ser um quantidade menor, é provável que haja menos riscos de efeitos colaterais. Segundo o diretor da SBIm, não há razões para não incluir essa faixa etária entre os grupos vacinados, “à medida que os dados sobre segurança e eficácia sejam submetidos à Anvisa”.
O pediatra Juarez Cunha, presidente da SBim, que também participou da coletiva da Pfizer ontem, reforçou a importância da inclusão do público infantil no grupo de vaicnados e definiu como “absurdo” o número de mortes – 2.400 – de crianças e adolescentes em todo o Brasil, dao. “É um numero muito maior do que todas as outras doenças preveníveis da infância, então o impacto nessa faixa etária, ao se protegerem e evitarem a transmissão, é muito importante”, alertou Cunha. Doenças preveniveis são todas aquelas possíveis de evitar, para as quais já existem vacinas previstas no calendário vacinal, como hepatite, rubéola e coqueluche, entre outras.
O presidente da Sbim lembrou que, segundo estudos, as crianças têm carga viral mais alta e transmitem mais. “Quanto maior a população que puder usar a vacina, incluindo crianças, será muito bem vindo”, destacou. Ele disse ainda que já há estudos da própria Pfizer para aplicação do imunizante em crianças abaixo dos 5 anos de idade, cujos resultados devem ser divulgados nos próximos meses.
LEIA TAMBÉM
[mc4wp_form id=”26137″]
Verônica Fraidenraich
Editora da Canguru News, cobre educação há mais de dez anos e tem interesse especial pelas áreas de educação infantil e desenvolvimento na primeira infância. Tem um filho, Martim, sua paixão e fonte diária de inspiração e aprendizados.
VER PERFILAviso de conteúdo
É proibida a reprodução do conteúdo desta página em qualquer meio, eletrônico ou impresso, sem autorização escrita. O site não se responsabiliza pelas opiniões dos autores deste coletivo.
Veja Também
“O belo caos do coração de uma mãe”: o que o discurso no Oscar nos lembra sobre a maternidade
Ao receber o Oscar por Hamnet, a atriz irlandesa definiu muito bem a contraditoriedade e a complexidade de emoções envolvidas...
Guerreiras do K-Pop: o que fez a animação virar fenômeno e brilhar no Oscar
Mistura de música, ação, fantasia e cultura coreana transformou a animação em um verdadeiro hit mundial entre as crianças e...
Febre: nem sempre é preciso correr para o pronto-socorro; entenda quando se preocupar
A elevação de temperatura assusta e deixa muitos pais aflitos, com medo de complicações, como a convulsão. No entanto, ela...
Mpox: o que os pais precisam saber sobre a doença e o risco para crianças no Brasil
Casos seguem sendo registrados no país, mas autoridades descartam surto. Entenda como ocorre a transmissão, quais são os sintomas nas...













